KOVALENT BAĞLAR
Hidrojenin ametallerle ya da ametallerin kendi aralarında elektronlarını ortaklaşa kullanarak oluşturulan bağa kovalent bağ denir.
a. Apolar Kovalet Bağ
Kutupsuz bağ, yani (+), (-) kutbu yoktur.
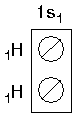
İki hidrojen atomu elektronları ortaklaşa kullanarak bağ oluştururlar.
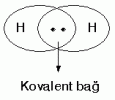
Elektron nokta yapısıyla;
şeklinde gösterilir. İki arasındaki bağ H—H şeklinde gösterilir ve H2 şeklinde yazılır.
Aynı cins atomlar arasındaki bağ apolar kovalent bağdır.
Elektronlar iki atom arasında eşit olarak paylaşılmadığından kutuplaşma oluşur ve buna polar kovalent bağ denir. Bu polarlığı HF molekülü ile açıklamaya çalışalım:
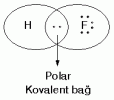
Hidrojen ve Flor elektron ortaklığı ile bileşik oluşturmuş durumdadır. Florun elektron alması yani elektronu kendisine çekme gücü hidrojenden daha fazla olduğundan elektron kısmen de olsa Flor tarafındadır. Dolayısıyle Flor kısmen (-), Hidrojen ise kısmen (+) yüklenmiş olur. Bu olaya kutuplaşma, bu tür bağa polar kovalent bağ denir.
Hidrojenin ametallerle ya da ametallerin kendi aralarında elektronlarını ortaklaşa kullanarak oluşturulan bağa kovalent bağ denir.
a. Apolar Kovalet Bağ
Kutupsuz bağ, yani (+), (-) kutbu yoktur.

İki hidrojen atomu elektronları ortaklaşa kullanarak bağ oluştururlar.

Elektron nokta yapısıyla;
şeklinde gösterilir. İki arasındaki bağ H—H şeklinde gösterilir ve H2 şeklinde yazılır.
Aynı cins atomlar arasındaki bağ apolar kovalent bağdır.
b. Polar Kovalent Bağlar
Farklı ametaller arasında oluşan bağa polar kovalent (kutuplu) bağ diyoruz.Elektronlar iki atom arasında eşit olarak paylaşılmadığından kutuplaşma oluşur ve buna polar kovalent bağ denir. Bu polarlığı HF molekülü ile açıklamaya çalışalım:

Hidrojen ve Flor elektron ortaklığı ile bileşik oluşturmuş durumdadır. Florun elektron alması yani elektronu kendisine çekme gücü hidrojenden daha fazla olduğundan elektron kısmen de olsa Flor tarafındadır. Dolayısıyle Flor kısmen (-), Hidrojen ise kısmen (+) yüklenmiş olur. Bu olaya kutuplaşma, bu tür bağa polar kovalent bağ denir.

